ВОЛГОГРАДСКАЯ ГОСУДАРСТВЕННАЯ АКАДЕМИЯ ФИЗИЧЕСКОЙ КУЛЬТУРЫ
Реферат
по биологии
на тему:
«Регенерация, ее виды и уровни. Условия, влияющие на течение восстановительных процессов»
Выполнил: студент группы 108
Тимофеев Д. М
Волгоград 2003
Введение
1. Понятие регенерации
2. Виды регенерации
3. Условия, влияющие на течение восстановительных процессов
Заключение
Список используемой литературы
Введение
Регенерация - обновление структур организма в процессе жизнедеятельности и восстановление тех структур, которые были утрачены в результате патологических процессов. В большей степени регенерация присуща растениям и беспозвоночным животным, в меньшей - позвоночным. Регенерация - в медицине - полное восстановление утраченных частей.
Явления регенерации были знакомы людям еще в глубокой древности. К концу 19 в. был накоплен материал,раскрывающий закономерности регенераторной реакции у человека и животных, но особенно интенсивно проблема регенрации разрабатывается с 40-х гг. 20 в.
Ученые давно пытаются понять, каким образом земноводные - например, тритоны и саламандры -- регенерируют оторванные хвосты, конечности, челюсти. Более того, у них восстанавливаются и поврежденное сердце, и глазные ткани, и спинной мозг. Способ, применяемый земноводными для саморемонта, стал понятен, когда ученые сравнили регенерацию зрелых особей и эмбрионов. Оказывается, на ранних стадиях развития клетки будущего существа незрелы, их участь вполне может измениться.
В данном реферате будут дано понятие и рассмотрены виды регенерации, а также особенности течения восстановительных процессов.
1. Понятие регенерации
РЕГЕНЕРАЦИЯ (от позднелат. regenera-tio -возрождение, возобновление) в биологии, восстановление организмом утраченных или повреждённых органов и тканей, а также восстановление целого организма из его части. Регенерация наблюдается в естественных условиях, а также может быть вызвана экспериментально.
Р егенерация у животных и человека - образование новых структур взамен удалённых либо погибших в результате повреждения (репаратинпая регенерация) или утраченных в процессе нормальной жизнедеятельности (физиологнческая регенерация); вторичное развитие, вызванное утратой развившегося ранее органа. Регенерировавший орган может иметь такое же строение, как удалённый, отличаться от него или совсем не походить на него (атипичная регенерация) .
Термин « регенерация» предложен в 1712 франц. учёным Р. Реомюром, изучавшим регенерацию ног речного рака. У многих беспозвоночных возможна регенерация целого организма из кусочка тела. У высокоорганизонанных животных это невозможно - регенерируют лишь отдельные органы или их части. Регенерация может происходить путём роста тканей на раневой поверхности, перестройки оставшейся части органа в новый или путём роста остатка органа без изменения его формы. Представление об ослаблении способности к регенерации по мере повышения организации животных ошибочно, т. к. процесс регенерации зависит не только от уровня организации животного, но и от многих других факторов и характеризуется значит, изменчивостью. Неправильно также утверждение, что способность к регенерации закономерно падает с возрастом; она может и повышаться в процессе онтогенеза, но в период старости часто наблюдают её снижение. За последнюю четверть века показано, что, хотя у млекопитающих и человека целые наружные органы не регенерируют, внутренние их органы, а также мышцы, скелет, кожа способны к регенерации, которую изучают на органном, тканевом, клеточном и субклеточном уровнях. Разработка методов усиления (стимуляции) слабой и восстановления утраченной способности к регенерации приблизит учение о регенерации к медицине.
Регенерация в медицине. Различают физиологическую, репаративную и патологическую регенерацию. При травмах и др. патологических состояниях, которые сопровождаются массовой гибелью клеток, восстановление тканей осуществляется за счёт репаративнои (восстановительной) регенерации. Если в процессе репаративной регенерации утраченная часть замещается равноценной, специализированной тканью, говорят о полной регенерации (реституции); если на месте дефекта разрастается неспециализированная соединительная ткань,- о неполной регенерации (заживлении посредством рубцевания). В ряде случаев при субституции функция восстанавливается за счёт интенсивного новообразования ткани (аналогичной погибшей) в неповреждённой части органа. Это новообразование происходит путём либо усиленного размножения клеток, либо за счёт внутриклеточной регенерации- восстановления субклеточных структур при неизменённом числе клеток (сердечная мышца, нервная ткань). Возраст, особенности обмена веществ, состояние нервной и эндокринной систем, питание, интенсивность кровообращения в повреждённой ткани, сопутствующие заболевания могут ослабить, усилить или качественно изменить процесс регенерации. В некоторых случаях это приводит к патологической регенерации. Её проявления: длительно незаживающие язвы, нарушения срастания переломов костей, избыточные разрастания тканей или переход одного типа ткани в другой. Лечебные воздействия на процесс регенерации заключаются в стимуляции полной и предотвращении патологической регенерации.
Р егенерация у растений может происходить на месте утраченной части (реституция) или на другом месте тела (репродукция). Весеннее восстановление листьев вместо опавших осенью - естественная регенерация типа репродукции. Обычно, однако, под регенерацией понимают лишь восстановление насильственно отторженных частей. При такой регенерации организм прежде всего использует основные пути нормального развития. Поэтому регенерация органов у растений происходит преимущественно путём репродукции: отнятые органы компенсируются развитием существующих или образующихся вновь метамерных заложений. Так, при отрезании верхушки побега усиленно развиваются боковые побеги. Растения или их части, развивающиеся не метамерно, легче регенерируют путём реституции, как и участки тканей. Например, поверхность ранения может покрыться так называемой раневой перидермой; рана на стволе или ветке может зарубцеваться наплывами (каллюсами). Размножение растений черенками - простейший случай регенерации, когда из небольшой вегетативной части восстанавливается целое растение.
Широко распространена регенерация и из отрезков корня, корневища или слоевища. Можно вырастить растения из листовых черенков, кусочков листа (например, у бегоний). У некоторых растений удавалась регенерация из изолированных клеток и даже из отдельных изолированных протопластов, а у некоторых видов сифоновых водорослей - из небольших участков их многоядерной протоплазмы. Молодой возраст растения обычно способствует регенерации, но на слишком ранних стадиях онтогенеза орган может оказаться неспособным к регенерации. Как биологическое приспособление, обеспечивающее зарастание ран, восстановление случайно утраченных органов, а нередко и вегетативное размножение, регенерация имеет большое значение для растениеводства, плодоводства, лесоводства, декоративного садоводства и др. Она даёт материал и для решения ряда теоретических проблем, в т. ч. и проблем развития организма. Большую роль в процессах регенерации играют ростовые вещества.
2. Виды регенерации
Различают два вида регенерации - физиологическую и репаративную.
Физиологическая регенерация - непрерывное обновление структур на клеточном (смена клеток крови, эпидермиса и др.) и внутриклеточном (обновление клеточных органелл) уровнях, которым обеспечивается функционирование органов и тканей.
Репаративная регенерация - процесс ликвидации структурных повреждений после действия патогенных факторов.
Оба вида регенерации не являются обособленными, не зависимыми друг от друга. Так, репаративная регенерация развертывается на базе физиологической, т. е. на основе тех же механизмов, и отличается лишь большей интенсивностью проявлений. Поэтому репаративную регенерацию следует рассматривать как нормальную реакцию организма на повреждение, характеризующуюся резким усилением физиологических механизмов воспроизведения специфических тканевых элементов того или иного органа.
Значение регенерации для организма определяется тем, что на основе клеточного и внутриклеточного обновления органов обеспечивается широкий диапазон приспособительных колебаний их функциональной активности в меняющихся условиях окружающей среды, а также восстановление и компенсация нарушенных под воздействием различных патогенных факторов функций .
Физиологическая и репаративная регенерации являются структурной основой всего разнообразия проявлений жизнедеятельности организма в норме и патологии.
Процесс регенерации развертывается на разных уровнях организации - системном, органном, тканевом, клеточном, внутриклеточном. Осуществляется он путем прямого и непрямого деления клеток, обновления внутриклеточных органелл и их размножения. Обновление внутриклеточных структур и их гиперплазия являются универсальной формой регенерации, присущей всем без исключения органам млекопитающих и человека. Она выражается либо в форме собственно внутриклеточной регенерации, когда после гибели части клетки ее строение восстанавливается за счет размножения сохранившихся органелл, либо в виде увеличения числа органелл (компенсаторная гиперплазия органелл) в одной клетке при гибели другой.
Различают три вида регенерации: физиологическую, репаративную и патологическую.
ь Физиологическая - естественное обновление структуры. В ходе жизнедеятельности на смену гибнущим клеткам приходят новые. В физиологической регенерации участвуют клетки всех обновляющихся популяций и образуемые ими тканевые структуры. Нет таких структур, которые не подвергались бы физиологической регенерации. Там, где доминирует клеточная форма регенерации, имеет место обновление клеток. Так происходит постоянная смена покровного эпителия кожи и слизистых оболочек, секреторного эпителия экзокринных желез, клеток, выстилающих серозные и синовиальные оболочки, клеточных элементов соединительной ткани, эритроцитов, лейкоцитов и тромбоцитов крови и т.д. В тканях и органах, где клеточная форма регенерации утрачена, например в сердце, головном мозге, происходит обновление внутриклеточных структур. Наряду с обновлением клеток и субклеточных структур постоянно совершаетсябиохимическая регенерация,т.е. обновление молекулярного состава всех компонентов тела.
Примером физиологической регенерации на внутриклеточном уровне являются процессы восстановления субклеточных структур в клетках всех тканей и органов. Значение ее особенно велико для так называемых вечных тканей, утративших способность к регенерации путем деления клеток. В первую очередь это относится к нервной ткани.
Примерами физиологической регенерации на клеточном и тканевом уровнях являются обновление эпидермиса кожи, роговицы глаза, эпителия слизистой кишечника, клеток периферической крови и др. Обновляются производные эпидермиса -- волосы и ногти. Это так называемая пролиферативная регенерация, т. е. восполнение численности клеток за счет их деления. Во многих тканях существуют специальные камбиальные клетки и очаги их пролиферации. Это крипты в эпителии тонкой кишки, костный мозг, пролиферативные зоны в эпителии кожи. Интенсивность клеточного обновления в перечисленных тканях очень велика. Это так называемые лабильные ткани. Все эритроциты теплокровных животных, например, сменяются за 2--4 месяца, а эпителий тонкой кишки полностью сменяется за 2 суток. Это время требуется для перемещения клетки из крипты на ворсинку, выполнения ею функции и гибели. Клетки таких органов, как печень, почка, надпочечник и др., обновляются значительно медленнее. Это так называемые стабильные ткани.
Об интенсивности пролиферации судят по количеству митозов, приходящихся на 1000 подсчитанных клеток. Если учесть, что сам митоз в среднем длится около 1 ч, а весь митотический цикл в соматических клетках в среднем протекает 22--24 ч, то становится ясно, что для определения интенсивности обновления клеточного состава тканей необходимо подсчитать количество митозов в течение одних или нескольких суток. Оказалось, что количество делящихся клеток не одинаково в разные часы суток. Так был открыт суточный ритм клеточных делений.
Суточный ритм количества митозов обнаружен не только в нормальных, но и в опухолевых тканях. Он является отражением более обшей закономерности, а именно ритмичности всех функций организма. Одна из современных областей биологии -- хронобиология -- изучает, в частности, механизмы регуляции суточных ритмов митотической активности, что имеет весьма важное значение для медицины. Существование самой суточной периодичности количества митозов указывает на регулируемость физиологической регенерации организмом. Кроме суточных существуют лунные и годичные циклы обновления тканей и органов.
В физиологической регенерации выделяют две фазы: разрушительную и восстановительную. Полагают, что продукты распада части клеток стимулируют пролиферацию других. Большую роль в регуляции клеточного обновления играют гормоны.
Физиологическая регенерация присуща организмам всех видов, но особенно интенсивно она протекает у теплокровных позвоночных, так как у них вообще очень высока интенсивность функционирования всех органов по сравнению с другими животными.
ь Репаративная регенерация- образование новых структур вместо повреждённых и на месте повреждённых. Признак репаративной регенерации - появление многочисленных малодифференцированных клеток со свойствами эмбриональных клеток зачатка регенерирующего органа или ткани. При репаративной регенерации какой-то структуры реконструируются процессы развития этой структуры в раннем онтогенезе. Репаративная регенерация может быть полной и неполной.
Полная регенерация, или реституция, характеризуется возмещением дефекта тканью, которая идентична погибшей. Она развивается преимущественно в тканях, где преобладает клеточная регенерация. Так, в соединительной ткани, костях, коже и слизистых оболочках даже относительно крупные дефекты органа могут путем деления клеток замещаться тканью, идентичной погибшей. При неполной регенерации, или субституции, дефект замещается соединительной тканью, рубцом. Субституция характерна для органов и тканей, в которых преобладает внутриклеточная форма регенерации, либо она сочетается с клеточной регенерацией. Поскольку при регенерации происходит восстановление структуры, способной к выполнению специализированной функции, смысл неполной регенерации не в замещении дефекта рубцом, а в компенсаторной гиперплазии элементов оставшейся специализированной ткани, масса которой увеличивается, т.е. происходит гипертрофия ткани.
При неполной регенерации, т.е. заживлении ткани рубцом, возникает гипертрофия как выражение регенераторного процесса, поэтому ее называют регенерационной, в ней - биологический смысл репаративной регенерации. Регенераторная гипертрофия может осуществляться двумя путями - с помощью гиперплазии клеток или гиперплазии и гипертрофии клеточных ультраструктур, т.е. гипертрофии клеток.
Существует несколько разновидностей или способов репаративной регенерации. К ним относят эпиморфоз, морфаллаксис, заживление эпителиальных ран, регенерационную гипертрофию, компенсаторную гипертрофию.
Ш Эпителизация при заживлении ран с нарушенным эпителиальным покровом идет примерно одинаково, независимо оттого, будет далее происходить регенерация органа путем эпиморфоза или нет. Эпидермальное заживление раны у млекопитающих в том случае, когда раневая поверхность высыхает с образованием корки, проходит следующим образом.
Рис. 3. Схема некоторых событий, происходящих при эпителизации кожной раны у млекопитающих. А -- начало врастания эпидермиса под некротическую ткань; Б -- срастание эпидермиса и отделение струпа: 1--соединительная ткань, 2--эпидермис, 3--струп, 4--некротическая ткань
Эпителий на краю раны утолщается вследствие увеличения объема клеток и расширения межклеточных пространств. Сгусток фибрина играет роль субстрата для миграции эпидермиса в глубь раны. В мигрирующих эпителиальных клетках нет митозов, однако они обладают фагоцитарной активностью. Клетки с противоположных краев вступают в контакт. Затем наступает кератинизация раневого эпидермиса и отделение корки, покрывающей рану.
К моменту встречи эпидермиса противоположных краев в клетках, расположенных непосредственно вокруг края раны, наблюдается вспышка митозов, которая затем постепенно падает. По одной из версий, эта вспышка вызвана понижением концентрации ингибитора митозов -- кейлона.
Ш Эпиморфоз представляет собой наиболее очевидный способ регенерации, заключающийся в отрастании нового органа от ампутационной поверхности. Регенерация конечности тритона и аксолотля изучена детально. Выделяют регрессивную и прогрессивную фазы регенерации. Регрессивная фаза начинается с заживления раны, во время которого происходят следующие основные события: остановка кровотечения, сокращение мягких тканей культи конечности, образование над раневой поверхностью сгустка фибрина и миграция эпидермиса, покрывающего ампутационную поверхность.
Затем начинается разрушение остеоцитов на дистальном конце кости и других клеток. Одновременно в разрушенные мягкие ткани проникают клетки, участвующие в воспалительном процессе, наблюдается фагоцитоз и местный отек. Затем вместо образования плотного сплетения волокон соединительной ткани, как это происходит при заживлении ран у млекопитающих, в области под раневым эпидермисом утрачиваются дифференцированные ткани. Характерна остеокластическая эрозия кости, что является гистологическим признаком дедифференцировки. Раневой эпидермис, уже пронизанный регенерирующими нервными волокнами, начинает быстро утолщаться. Промежутки между тканями все более заполняются мезенхимоподобными клетками. Скопление мезенхимных клеток под раневым эпидермисом является главным показателем формирования регенерационной бластемы. Клетки бластемы выглядят одинаково, но именно в этот момент закладываются основные черты регенерирующей конечности.
Затем начинается прогрессивная фаза, для которой наиболее характерны процессы роста и морфогенеза. Длина и масса регенерационной бластемы быстро увеличиваются. Рост бластемы происходит на фоне идущего полным ходом формирования черт конечности, т. е. ее морфогенеза. Когда форма конечности в общих чертах уже сложилась, регенерат все еще меньше нормальной конечности. Чем крупнее животное, тем больше эта разница в размерах. Для завершения морфогенеза требуется время, по истечении которого регенерат достигает размеров нормальной конечности.
Некоторые стадии регенерации передней конечности у тритона после ампутации на уровне плеча показаны на рисунке 4.
Время, необходимое для полной регенерации конечности, варьирует в зависимости от размера и возраста животного, а также от температуры, при которой она протекает.

Рис. 4.
У молодых личинок аксолотлей конечность может регенерировать за 3 нед, у взрослых тритонов и аксолотлей за 1--2 мес, а у наземных амбистом для этого требуется около 1 года.
При эпиморфной регенерации не всегда образуется точная копия удаленной структуры. Такую регенерацию называют атипичной. Существует много разновидностей атипичной регенерации:
· Гипоморфоз -- регенерация с частичным замещением ампутированной структуры. Так, у взрослой шпорцевой лягушки возникает шиловидная структура вместо конечности.
· Гетероморфоз -- появление иной структуры на месте утраченной. Это может проявляться в виде гомеозисной регенерации, заключающейся в появлении конечности на месте антенн или глаза у членистоногих, а также в изменении полярности структуры. Из короткого фрагмента планарии можно стабильно получать биполярную планарию (рис.5.).
Рис.5.
Встречается образование дополнительных структур, или избыточная регенерация. После надреза культи при ампутации головного отдела планарии возникает регенерация двух голов или более (рис.6.). Можно получить больше пальцев при регенерации конечности аксолотля, повернув конец культи конечности на 180°. Дополнительные структуры являются зеркальным отражением исходных или регенерировавших структур, рядом с которыми они расположены (закон Бэйтсона).

Рис.6.
Ш Морфаллаксис -- это регенерация путем перестройки регенерирующего участка. Примером служит регенерация гидры из кольца, вырезанного из середины ее тела, или восстановление планарии из одной десятой или двадцатой ее части. На раневой поверхности в этом случае не происходит значительных формообразовательных процессов. Отрезанный кусочек сжимается, клетки внутри него перестраиваются, и возникает целая особь уменьшенных размеров, которая затем растет. Этот способ регенерации впервые описал Т. Морган в 1900 г. В соответствии с его описанием морфаллаксис осуществляется без митозов. Нередко имеет место сочетание эпиморфного роста на месте ампутации с реорганизацией путем морфаллаксиса в прилежащих частях тела.
Ш Регенерационная гипертрофия относится к внутренним органам. Этот способ регенерации заключается в увеличении размеров остатка органа без восстановления исходной формы. Иллюстрацией служит регенерация печени позвоночных, в том числе млекопитающих. При краевом ранении печени удаленная часть органа никогда не восстанавливается. Раневая поверхность заживает. В тоже время внутри оставшейся части усиливается размножение клеток (гиперплазия) и в течение двух недель после удаления 2 /з печени восстанавливаются исходные масса и объем, но не форма. Внутренняя структура печени оказывается нормальной, дольки имеют типичную для них величину. Функция печени также возвращается к норме.
Ш Компенсаторная гипертрофия заключается в изменениях в одном из органов при нарушении в другом, относящемся к той же системе органов. Примером является гипертрофия в одной из почек при удалении другой или увеличение лимфатических узлов при удалении селезенки.
Последние два способа отличаются местом регенерации, но механизмы их одинаковы: гиперплазия и гипертрофия.
ь Опатологической регенерации говорят в тех случаях, когда в результате тех или иных причин имеется извращение регенераторного процесса, нарушение смены фазпролиферации и дифференцировки. Патологическая регенерация проявляется в избыточном или недостаточном образовании регенерирующей ткани (гипер- или гипорегенерация), а также в превращении в ходе регенерации одного вида ткани в другой. Примерами могут служить гиперпродукция соединительной ткани с образованием келоида, избыточная регенерация периферических нервов и избыточное образование костной мозоли при срастании перелома, вялое заживление ран и метаплазия эпителия в очаге хронического воспаления. Патологическая регенерация обычно развивается при нарушениях общих и местных условий регенерации(нарушение иннервации, белковое и витаминное голодание, хроническое воспаление и т.д.).
Регуляция регенераторного процесса. Среди регуляторных механизмов регенерации различают гуморальные, иммунологические, нервные, функциональные.
ь Гуморальные механизмы реализуются как в клетках поврежденных органов и тканей (внутритканевые и внутриклеточные регуляторы), так и за их пределами (гормоны, поэтины, медиаторы, факторы роста и др.). К гуморальным регуляторам относят кейлоны (от греч. chalaino- ослаблять) - вещества, способные подавлять деление клеток и синтез ДНК; они обладают тканевой специфичностью.
ь Иммунологические механизмы регуляции связаны с «регенерационной информацией», переносимой лимфоцитами. В связи с этим следует заметить, что механизмы иммунологического гомеостаза определяют и структурный гомеостаз.
ь Нервные механизмы регенераторных процессов связаны прежде всего с трофической функцией нервной системы, афункциональные механизмы- с функциональным «запросом» органа, ткани, который рассматривается как стимул к регенерации.
Развитие регенераторного процесса во многом зависит от ряда общих и местных условий, или факторов. К общим следует отнести возраст, конституцию, характер питания, состояние обмена и кроветворения, к местным- состояние иннервации, крово- и лимфообращения ткани, пролиферативную активность ее клеток, характер патологического процесса.
Регенерация – процесс вторичного развития органа или ткани, вызванный повреждениями какого – либо рода.
Регенерация происходит на всех уровнях материи
По способности к регенерации выделяют 3 группы тканей и органов:
1. Регенераторная реакция в форме новообразования клеток: эпителий кожи, костный мозг, костная ткань, эпителий тонкой кишки, лимфатическая система.
2. Промежуточная форма. Происходит деление клеток и внутриклеточная регенерация. Печень, легкие, почки, надпочечники, скелетная мускулатура.
3. Преобладает внутриклеточная регенерация. Клетки центральной нервной системы, миокарда.
Физиологическая регенерация – восстановление частей организма, износившихся в процессе жизнедеятельности. Действует на протяжении всего онтогенеза, поддерживает постоянство структур, несмотря на гибель клеток. Интенсивные процессы физиологической регенерации при восстановлении клеток крови, эпидермиса, слизистых оболочек. Примерами могут быть линька птиц, рост зубов у грызунов. Физиологическая регенерация происходит не только в тканях с интенсивно делящимися клетками, но и там, где клетки делятся незначительно. 25 гепатоцитов из 1000 погибают и столько же восстанавливаются. Физиологическая регенерация – динамический процесс, который включает в себя клеточное деление и другие процессы. Обеспечение функций лежит в основе нормального функционирования организма.
Физиологическая регенерация представляет собой процесс обновления функционирующих структур организма. Благодаря физиологической регенерации поддерживается структурный гомеостаз и обеспечивается возможность постоянного выполнения органами их функций. С общебиологической точки зрения, физиологическая регенерация, как и обмен веществ, является проявлением такого важнейшего свойства жизни, как самообновление.
Примерами физиологической регенерации на клеточном и тканевом уровнях являются обновление эпидермиса кожи, роговицы глаза, эпителия слизистой кишечника, клеток периферической крови и др.
Обновляются производные эпидермиса - волосы и ногти. Это так называемая пролиферативная регенерация, т.е. восполнение численности клеток за счет их деления.
В физиологической регенерации выделяют две фазы: разрушительную и восстановительную. Полагают, что продукты распада части клеток стимулируют пролиферацию других. Большую роль в регуляции клеточного обновления играют гормоны.
Репаратиная регенерация,ее значение.Способы репаративной регенерации. Проявление регенерационной способности в филогенезе. Молекулярно- генетические, клеточные и системные механизмы регенерации. Особенности восстановительных процессов у млекопитающих.
Репаративная (восстановительная) регенерация – восстановление поврежденных тканей и органов после чрезвычайных воздействий. При полной регенерации восстанавливается полное исходное строение ткани после ее повреждения, её архитектура остается неизменной. Распространена у организмов, способных к бесполому размножению. Например, белая планария, гидра, моллюски (если удалить голову, но оставить нервно – узловую структуру). Типичная репаративная регенерация возможна у высших организмов, в т.ч. и человека. Например, при устранении некротических клеток органов. В острой стадии пневмонии происходит деструкция альвеол и бронхов, затем происходит восстановление. При действии гепатотропных ядов возникают диффузные некротические изменения печени. После прекращения действия ядов восстанавливается архитектоника за счет деления гепатоцитов – клеток печеночной паренхимы. Восстанавливается исходная структура.Гомоморфоз – восстановление структуры в том виде, в котором она существовала до разрушения. Неполная репаративная регенерация – регенерированный орган отличается от удаленного - гетероморфоз . Исходная структура не восстанавливается, а иногда вместо одного органа развивается другой орган. Например, глаз у рака. При удалении в некоторых случаях развивается антенна. У человека печень при удалении части печеночной доли аналогично регенерирует. Возникает рубец и через 2 - 3 месяца после операции масса печени восстанавливается, а восстановления формы органа не происходит. Это происходит из-за удаления и повреждения соединительной ткани во время операции.
Избыточная регенерация - образование дополнительных структур. После надреза культи при ампутации головного отдела планарии возникает регенерация двух голов или более.
У млекопитающих могут регенерировать все 4 вида ткани:
1. Соединительная ткань . Рыхлая соединительная ткань обладает высокой способностью к регенерации. Лучше всего регенерируют интерстициальные компоненты – образуется рубец, замещающийся тканью. Костная ткань – аналогично. Основные элементы, восстанавливающие ткань – остеобласты (малодифференцированные камбиальные клетки костной ткани);
2. Эпителиальная ткань . Обладает выраженной регенерационной реакцией. Эпителий кожи, роговая оболочка глаза, слизистые оболочки полости рта, губ, носа, желудочно-кишечного тракта, мочевого пузыря, слюнные железы, паренхима почек. При наличии раздражающих факторов могут происходить патологические процессы, приводящие к разрастанию тканей, что приводит к раковым опухолям.
3. Мышечная ткань . Значительно меньше регенерирует, чем эпителиальная и соединительная ткани. Поперечная мускулатура – амитоз, гладкая – митоз. Регенерирует за счет недифференцированных клеток – сателлитов. Могут разрастаться и регенерировать отдельные волокна, и даже целые мышцы.
4. Нервная ткань . Обладает плохой способностью к регенерации. В эксперименте показано, что клетки периферической и вегетативной нервной системы, двигательные и чувствительные нейроны в спинном мозге мало регенерируют. Аксоны хорошо регенерируют за счет Шванновских клеток. В головном мозге вместо них - глия, поэтому регенерация не происходит.
способы репаративной регенерации :
· Эпителизация -заживление эпителиальных ран.
· Эпиморфоз - отрастание нового органа от ампутационной поверхности
· Морфоллаксис – регенерация путём перестройки регенерирующего участка (Примером служит регенерация гидры из кольца, вырезанного из середины ее тела, или восстановление планарии из одной десятой или двадцатой ее части.)
· Регенерационная гипертрофия - к внутренним органам. Этот способ регенерации заключается в увеличении размеров остатка органа без восстановления исходной формы.(регенерация печени(гипеоплазия), восстанавливаются исходные функция, масса и объем, но не форма)
· Компенсаторная гипертрофия -заключается в изменениях в одном из органов при нарушении в другом, относящемся к той же системе органов. (гипертрофия в одной из почек при удалении другой или увеличение лимфатических узлов при удалении селезенки.)
Биологическое и медицинское значение проблемы регенерации. Проявление регенерационной способности у человека.Ренерация патологически измененных органов и обратимость патологически изменённых органов.Регенерационная терапия.
При разрезе в рану устремляется кровь, лейкоциты которой запускают воспалительный процесс. Клетки прилежащей эпителиальной ткани делятся и образуют «струп» (рубец). Потом начинается процесс заживления.
В настоящее время интенсивно изучаются проблемы регенерации, особенно связанные с медициной. Стволовые клетки обладают свойствами :
Стволовая клетка не является окончательно дифференцированной (она скорее детерминирована);
Стволовая клетка способна к неограниченному делению;
При делении часть клеток остается стволовыми, другая часть подвергается процессу дифференцировки.
Центров по применению стволовых клеток очень мало, в России существует только 2 таких центра. Однако стволовые клетки есть везде. Для лечения и экспериментов берется пуповинная кровь с целью получения стволовых клеток.
Кости черепа в норме не регенерируют. Под руководством И.И.Полежаева происходило удаление участка 10х10 см черепа собаки. Из кости получали путем измельчения костные опилки, которые помещали на рану. В другом эксперименте использовали костные опилки донора и кровь реципиента. Через неделю происходило рассасывание опилок, а к концу 1 года рана зарастала.
Большое значение имеет регенерация после радиоактивного облучения. Малые дозы стимулируют, а большие, наоборот ингибируют данный процесс.
Если провести механическое раздавливание культи или помещение ее в кислоту – регенерация идет в 50% случаев.
Елизаров проводил ломку и удлинение костей. Им были созданы уникальные аппараты, благодаря которым было возможно раздвижение костей скелета и коррекция их формы.
Остро стоит проблема регенерации печени. При циррозе печени приходится проводить ее частичное удаление. Иногда подобная операция проводится несколько раз, печень быстро регенерирует без сохранения формы, сохраняя функцию и общую массу.
Регенерацию можно стимулировать антикейлоном, витамином В12, АТФ, РНК.
Выделяют типы регенерации в патологически измененных органах.
Регенерация после воздействия токсических веществ.
Регенерация после воздействия вредных физических факторов.
Регенерация после заболеваний, вызываемых микроорганизмами и вирусами.
Регенерация после нарушения кровоснабжения.
Регенерация после голода, гипокинезии (обездвиживании), атрофии.
Регенерация после повреждений, вызываемых в организме нарушением функции органов.
78.Понятие о гомеостазе. Общие закономерности гомеостаза живых систем. Генетические, клеточные и системные основы гомеостатических реакций организма. Роль эндокринной, нервной и иммунной систем в обеспечении гомеостаза и адаптивных изменений.
Термин «гомеостаз» был предложен для понимания постоянства состава лимфы, крови и тканевой жидкости. Гомеостаз характерен для любой системы, это своего рода обобщение множества частных проявлений стабильности системы.
Гомеостаз – поддержание постоянства внутренней среды организма в непрерывно изменяющихся условиях внешней среды. Т.к. организм – многоуровневый саморегулирующийся объект, его можно рассматривать с точки зрения кибернетики. Тогда, организм – сложная многоуровневая саморегулирующаяся система с множеством переменных.
Переменные входа:
Причина;
Раздражение.
Переменные выхода:
Реакция;
Следствие.
Причина – отклонение от нормы реакции в организме. Решающая роль принадлежит обратной связи. Существует положительная и отрицательная обратная связь.
Отрицательная обратная связь уменьшает действие входного сигнала на выходной. Положительная обратная связь увеличивает действие входного сигнала на выходной эффект действия.
Живой организм – ультрастабильная система, осуществляющая поиск наиболее оптимального устойчивого состояния, которое обеспечивается адаптациями.
Адаптация – поддержание переменных показателей на поведенческом, анатомическом, биохимическом и других уровнях.
Этология – наука, изучающая поведение животных и человека. Типы поведения животных и человека ограничены их морфологическими и физиологическими особенностями. У человека есть зависимость поведения от типа сложения. Существуют 3 типа сложения:
эндоморфный;
эктоморфный;
мезоморфный.
Животные могут совершенствовать свои движения за счет информации, кроме того, они имеют возможность регулировать их. Животные должны различать объекты внешней среды, получать информацию при помощи органов чувств. Полученная информация подвергается переработке нервной и эндокринной системами. Многие типы поведения могут вызывать гормональные изменения.
Морфологические и физиологические признаки подвержены естественному отбору, поведение в свою очередь, зависит от этих признаков, а значит, зависит и от естественного отбора. Поведение передается по наследству, повышает приспособляемость, увеличивает продолжительность жизни, количество потомков. Различные поведенческие реакции позволяют использовать благоприятные условия среды, защищают организм от неблагоприятных условий. Например, у пчел поддержание чистоты в улье. За гигиеническое поведение отвечают как минимум 2 гена. Поддержание чистоты защищает пчел от болезней. Поведение ящерицы, отбрасывающей хвост, если это необходимо, - тоже приспособительная реакция. Другие типы поведенческих реакций наблюдаются при защите от хищников, при поиске пищи, партнера, защите потомства и многих других случаях. Некоторые насекомые выделяют особые химические вещества – феромоны для привлечения потомства. В брачный период лягушки квакают и их «песня» видоспецифична.
Поведенческие признаки обладают не только адаптивными свойствами, но могут также и наследоваться, что обусловливает естественный отбор. Не все типы поведения получаются при передаче с генами, они могут приобретаться – благоприобретенные. Резкую границу между теми и другими провести нельзя, т.к. гены и среда тесно взаимодействуют друг с другом, поэтому выделить отдельно генетические и благоприобретенные свойства нельзя.
Можно привести следующие примеры генетических свойств. Хорея Гентингтона – наследственное заболевание, «танец», поражает ЦНС, у больных также нарушена пространственная ориентация. Другой пример, дауны бывают благожелательными, ласковыми, подражают действиям здоровых людей
Итак, важные свойства поведенческих реакций :
Поведение подвержено действию естественного отбора;
Поведенческие признак возникают из анатомии, морфологии и физиологии животного неотделимы о них;
Формы поведения обычно адаптивны и часто могут передаваться либо генетически, либо в результате обучения;
У многих биологических видов существуют определенные формы поведения.
Если организм не смог адаптироваться на поведенческом уровне, он делает это на биохимическом уровне. Биохимическая адаптация очень сложна, наиболее характерна для растений, т.к. животному проще мигрировать.
Процесс адаптации бывает по времени:
Эволюционная адаптация;
Акклиматизация;
Немедленная адаптация.
Эволюционная адаптация – длительный процесс, приобретение новой генетической информации, изменяется генотип, следовательно, изменяется и фенотип. Для своего завершения подобная адаптация требует многих поколений.
Акклиматизация – адаптации, которые происходят в процессе жизни в естественных условиях.
Акклимация – адаптации, происходящие в искусственных условиях.
Происходит в течение нескольких часов – лет (зима – лето). Смена часовых поясов, перевод времени.
Немедленная адаптация сопровождается почти мгновенной адаптивной реакцией (психогенное воздействие, переход из тепла в холод). Кратковременная реакция.
Любая адаптация возникает в результате взаимодействия генетических факторов и факторов внешней среды.
Генетический аспект гомеостаза рассматривают с 3 позиций:
Гомеостаз генотипа;
Гомеостаз организма как целого. Контроль за единством генотипа всего организма. Поддержание гомеостаза осуществляется при гибели видоизмененных клеток.
Гомеостаз популяции. Закон генетической стабильности в популяции.
В поддержании гомеостаза участвуют различные системы.
Нервная сигнализация – основной инструмент передачи и оценки сигналов из внутренней и внешней среды.
Гормоны принимают участие в регуляции гомеостаза. Регулируют обмен веществ, воды, белков, липидов, углеводов, энергии, электролитов. Контролируют работу всех органов, в том числе почек, печени, ЦНС.
Иммунная система защищает постоянство внутренней среды организма от факторов 2-х групп:
Микроорганизмов и экзогенных факторов с признаками чужеродной генетической информацией;
Соматических мутаций. Достаточно изменений в 1-2 генах, чтобы сработала иммунная система.
79.Проблемы трансплантации органов и тканей. Ауто-, алло- и ксенотрансплантация, трансплантация жизненно важных органов. Иммунитет. Тканевая несовместимость и пути ее преодоления. Искусственные органы.
Из-за бурного развития трансплантологии остро встал вопрос о трансплантационном иммунитете.
Трансплантология – медико-биологическая наука, изучающая вопросы заготовки, консервирования и пересадки органов и тканей.
Трансплантационный иммунитет – своеобразная реакция организма на трансплантацию, проявляющаяся в отторжении пересаженных органов и тканей.
Классификация терминов (Вена, 1967 год).
Трансплантат – пересаживаемая ткань или орган.
Реципиент – тот, кому пересаживается орган или ткань.
Донор – тот, от кого берут трансплантат.
Аутотрансплантация – пересадка тканей и органов в пределах одного организма (в таком случае говорят об аутотрансплантате)
Изотрансплантация (изотрансплантат) - пересадка тканей и органов между организмами, идентичными по генетическим признакам.
Аллотранспланация (аллотрансплантат) - пересадка тканей и органов между организмами одного биологического вида.
Ксенотрансплантация (ксенотрансплантат) – пересадка тканей и органов между организмами разных биологических видов.
Эксплантация (эксплантат) – пересадка небиологического материала.
Комбинированная пересадка (комбинированный трансплантат).
Остро стоят 2 проблемы: сохранение органов и тканей с их неизмененными свойствами. Другая проблема – преодоление трансплантационного иммунитета.
Разные методы консервации .
1) Охлаждение (недолговременное).
2) Замораживание.
3) Лиофилизации.
Заморозка может разорвать ткань, что приводит к гибели ткани. Но сперматозоиды способны жить. Состояние анабиоза некоторых животных. Кровь заменяют криопротекторами, после разморозки производят обратную замену. Метод лиофилизации – заморозка высушиванием в воздухе. Хранение замороженных людей. Существуют банки тканей, банки органов на научной основе.
Преодоление тканевой несовместимости – работа хирургов, иммунологов, физиологов и других специалистов. Целое медицинское направление - иммунодепрессивная терапия – направлено на решение этой проблемы. Используют химические, физические и биологические факторы воздействия на организм реципиента.
Физические методы – радиоактивное излучение, рентгеновские лучи.
Химические методы – введение препаратов, снижающих иммунитет. Они сильно влияют на жизненно важные органы.
Биологические методы – введение антитоксических сывороток, антибиотиков. Принцип действия - нейтрализация трансплантационных антител. Наиболее перспективный метод.
В настоящее время пересаживают практически все: и органы, и ткани.
История трансплантологии в России.
1933 – Ю.воронов – первая в мире пересадка почки.
1937 год – Демихов - первая в СССР пересадка сердца собаке.
1946 – Демихов – пересадил сердце и легкие собаке.
1948 – Демихов, Швековский – пересадка печени собаке.
1954 – Демихов пересадил вторую голову собаке.
1965 – Петровский – первая успешная пересадка почки.
1986 – Шумаков – первая в СССР пересадка сердца человеку.(1967 – Кристиан Бернард – ЮАР – успешная пересадка сердца человеку).
1990 – Ерамишанцев – первая в СССР пересадка печени человеку.
В Воронеже существует центр по пересадке почек. В клинике Шарите в Германии ежегодно делаются 60-100 операций по пересадке печени.
В 2005 году в Англии произведена успешная операция по пересадки печени от одного донора – ребенку и взрослому человеку.
Несмотря на заслуги, трансплантология ограничена законодательством, кроме того, многие органы являются «дефицитными».
80.Биологические ритмы. Хронобиология и хрономедицина.
Наука, изучающая биоритмы – биоритмология .
Биологический ритм - колебание ритма или скорости какого-либо биологического процесса, наступающее примерно через равные промежутки времени. Биологические ритмы присущи всем живым организмам.
С точки зрения взаимодействия организма и среды выделяют:
- адаптивные ритмы (экологические). Колебания с периодами, близкими основным геофизическим ритмам. (лунные, годовые, сезонные, приливно-отливные ритмы).
- физиологические (рабочие) ритмы.
Колебания, отражающие деятельности рабочих систем органов организма.
Классификация биоритмов.
1. Ритмы высокой частоты.
Колебания совершаются с периодом от долей секунды до 30 минут. Ритмы ЭКГ, сокращения сердца, дыхания, перистальтики ЖКТ.
Ритмы средней частоты.
От 30 минут до 28 часов.
· ультрадианные -до 20 часов. (чередование быстрого и медленного сна.Оральное поведение.)
· циркадные 20-28 часов. Это видоизмененные суточные ритмы. Они врожденные, эндогенные, обусловленные свойствами организма и его генотипа. Обнаружены у всех организмов. (кровяное давление, пульс, изменение температуры тела)
Мезоритмы.
· инфрадианные -28 часов-6 суток. (рост бороды, сокращения сердца)
· циркасептальные -около 7 суток.(комары откладывают яйца через 7 дней, активность гормонов эпифиза, смертность от неинфекционных заболеваний, отторжение и приживание трансплантата.)
Макроритмы
20 дней – год
Мегаритмы.
Периоды в десятки лет.
Из всего разнообразия ритмических процессов основное внимание сосредоточено на суточных и сезонных ритмах. Суточная и сезонная ритмичность происходит на всех уровнях биологических реакций. Ритмы служат 2-м целям: приспособление организмов к ожидаемым условиям среды, составление уникальной системы времени, интеграция всех ритмов воедино.
Понятие цикла подразумевает периодичность процесса. Время между одинаковыми состояниями соседних ритмов – период Т . Число циклов в единицу времени – частота . Величина, которая соответствует среднему значению полезного сигнала – мезер. Наибольшее отклонение от мезера - амплитуда . Момент времени, когда регистрируется конкретная величина – фаза. Момент наибольшего поднятия – акрофаза , момент наименьшего поднятия – батифаза.
Заболевания, связанные с нарушениями биологических ритмов – десинхронозы .
Могут быть явные и скрытые.
Явный десинхроноз отличается присутствием упадка сил, быстрой утомляемостью, учащением пульса, артериального давления, дыхания.
Скрытый десинхроноз приводит к дискомфорту, нарушениям сна и аппетита. Это предболезненноле состояние.
тотальный десинхроноз . При этом происходят общие изменения всех систем органов.
частичный десинхроноз , в этом случае имеют место сбои отдельных органов и их функций.
Хронический десинхроноз происходит из-за частого отступления от привычного режима жизни.
Острый – возникает из-за сильного, грубого нарушения режима труда и отдыха, сна, питания. Самый резкий наблюдается у детей и стариков.
Ритмичность первоначально возникает в результате периодического воздействия окружающей среды, затем закрепляются генетически.
Из биоритмологии выделились:
Хронобиология;
Хронопатология;
Хронодиагностика;
Хронотерапия;
Хронофармакология (прием препаратов в определенное время);
Хроногигиена (соблюдение режима труда отдыха).
Хронобиология - раздел биологии, изучающий биологические ритмы, протекание различных биологических процессов (преимущественно циклических) во времени.
Хрономедицина – использование закономерностей биоритмов для улучшения профилактики,диагностики и лечения болезней человека.
81.Биологическая эволюция. Современные теории эволюции.
Принципы эволюции (по Ламарку)
В основе биологической эволюции лежат процессы самовоспроизведения макромолекул и организмов.
Биологическая эволюция – необратимое и направленное историческое развитие живой природы, она сопровождается:
Изменением генетического состава популяции;
Формированием адаптаций;
Образованием и вымиранием видов;
Преобразованием экосистем и биосферы в целом.
Восстановление структуры и функции может осуществляться с помощью клеточных или внутриклеточных гиперпластических процессов. На этом основании различают клеточную и внутриклеточную формы регенерации. Для клеточной формырегенерации характерно размножение клеток митотическим и амитотическим путем, для внутриклеточной – увеличение числа (гиперплазия) и размеров (гипертрофия) ультраструктур (ядра, ядрышек, митохондрий, рибосом, пластинчатого комплекса и т.д.) и их компонентов.
Внутриклеточная форма регенерации является универсальной, так как она свойственна всем органам и тканям. Однако структурно-функциональная специализация органов и тканей в фило - и онтогенезе «отобрала» для одних преимущественно клеточную форму, для других – преимущественно или исключительно внутриклеточную, для третьих – в равной мере обе формы регенерации. Преобладание той или иной формы регенерации в определенных органах и тканях определяется их функциональным назначением, структурно-функциональной специализацией. Необходимость сохранения целостности покровов тела объясняет, например, преобладание клеточной формы регенерации эпителия кожи и слизистых оболочек (см. схему).
Морфогенез регенераторного процесса складывается из двух фаз – пролиферации и дифференцировки. В фазу пролиферации размножаются молодые, недифференцированные клетки. Эти клетки называют камбиальными(от лат. cambium – обмен, смена), стволовыми клетками и клетками-предшественниками.
 |  |
||||
Для каждой ткани характерны свои камбиальные клетки, которые отличаются степенью пролиферативной активности и специализации, однако одна стволовая клетка может быть родоначальником нескольких видов клеток (например, стволовая клетка кроветворной системы, лимфоидной ткани, некоторые клеточные представители соединительной ткани).
В фазу дифференцировкимолодые клетки созревают, происходит их структурно-функциональная специализация.
Развитие регенераторного процесса во многом зависит от ряда общих и местных условий, или факторов. К общим следует отнести возраст, конституцию, характер питания, состояние обмена и кроветворения, к местным – состояние иннервации, крово- и лимфообращения ткани, пролиферативную активность ее клеток, характер патологического процесса.
ВИДЫ РЕГЕНЕРАЦИИ
Различают три основных вида регенерации:
Физиологическая;
Репаративная;
Патологическая.
Физиологическая регенерация – восстановление всех элементов, погибших в процессе жизнедеятельности вне патологии. Физиологическая регенерация совершается в течение всей жизни и характеризуется постоянным обновлением клеток, волокнистых структур, основного вещества соединительной ткани.
Репаративная регенерация – восстановление структур поврежденных или погибших в результате патологии. Полное восстановление называется реституция. Она развивается преимущественно в тканях, где преобладает клеточная регенерация. Так, в соединительной ткани, костях, коже и слизистых оболочках даже относительно крупные дефекты органа могут путем деления клеток замещаться тканью, идентичной погибшей. Нередко регенерация завершается рубцеванием – замещением утраченных тканей грануляционной, а затем фиброзной тканью с образованием рубца. Неполное восстановление с замещением погибших структур соединительнотканным рубцом – субституция характерна для органов и тканей, в которых преобладает внутриклеточная форма регенерации, либо она сочетается с клеточной регенерацией.
Регенерация физиологическая и репаративная – явление универсальное, свойственное не только тканям и клеткам, но и внутриклеточному, молекулярному уровням (регенерация повреждённой структуры ДНК).
Патологическая регенерация (дисрегенерация). Отражает процессы перестройки тканей и проявляется в том, что образуется ткань, не полностью соответствующая утраченной и при этом функция регенерирующей ткани не восстанавливается или извращается. О патологической регенерации говорят в тех случаях, когда в результате тех или иных причин имеется нарушение смены фаз пролиферации и дифференцировки. Патологическая регенерация представлена четырьмя видами:
Гипорегенерация;
Гиперрегенерация;
Метаплазия;
Дисплазия.
Гипорегенерация – недостаточная, медленная или остановившаяся регенерация (при трофических язвах, пролежнях).
Гиперрегенерация проявляется в том, что ткань регенерирует избыточно и при этом функция органа страдает (образование келоидного рубца, избыточная регенерация периферических нервов и избыточное образование костной мозоли при срастании перелома).
Метаплазия (от греч. metaplasso – превращать) – переход одного вида ткани в другой, гистогенетически родственный ей вид. Метаплазия чаще встречается в эпителии и соединительной ткани. Метаплазия эпителия может проявляться в виде перехода призматического эпителия в ороговевающий плоский (эпидермизация, или плоскоэпителиальная, метаплазия). Она наблюдается в дыхательных путях при хроническом воспалении, при недостатке витамина А, в поджелудочной, предстательной и других железах. Переход многослойного неороговевающего плоского эпителия в цилиндрический носит название прозоплазии. Возможна метаплазия эпителия желудка в кишечный эпителий (кишечная метаплазия или энтеролизация слизистой оболочки желудка), а также метаплазия эпителия кишки в желудочный эпителий (желудочная метаплазия слизистой оболочки кишки).
Метаплазия соединительной ткани с образованием хряща и кости встречается в рубцах, в стенке аорты (при атеросклерозе), в строме мышц, в капсуле заживших очагов первичного туберкулеза, в строме опухолей.
Метаплазия эпителия может быть фоном для развития раковой опухоли.
Дисплазия (от греч. dys – нарушение + plaseo – образую) – патологическая регенерация с развитием клеточной атипии и нарушением гистоархитектоники. Клеточная атипия представлена различной величиной и формой клеток, увеличением размеров ядер и их гиперхромией, увеличением числа фигур митоза, появлением атипичных митозов. Нарушения гистоархитектоники при дисплазии проявляются потерей полярности эпителия, а иногда и тех его черт, которые характерны для данной ткани или данного органа.
В соответствии со степенью пролиферации и выраженностью клеточной и тканевой атипии выделяют три стадии (степени) дисплазии: I – легкая; II – умеренная; III – тяжелая.
Дисплазия встречается главным образом при воспалительных и регенераторных процессах, отражая нарушение пролиферации и дифференцировки клеток. Ее начальные стадии (I-II) трудно отличимы от репаративной регенерации, они чаще всего обратимы. Изменения при тяжелой дисплазии (III стадия) значительно реже подвергаются обратному развитию и рассматриваются как предраковые – предрак. Поскольку дисплазию III степени практически невозможно отличить от карциномы in situ («рак на месте»), в последнее время дисплазию называют внутриэпителиальной неоплазией.
АТРОФИЯ
__________________________________________________________________
Атрофия (а – исключение, греч. trophe – питание) – прижизненное уменьшение объема клеток, тканей, органов со снижением их функции.
Не всякое уменьшение органа относится к атрофии. В связи с нарушениями в ходе онтогенеза орган может полностью отсутствовать – агенезия, сохранять вид раннего зачатка – аплазия, не достигать полного развития – гипоплазия. Если наблюдается уменьшение всех органов и общее недоразвитие всех систем организма, говорят о карликовом росте.
Атрофию делят на физиологическую и патологическую.
Общие сведения
Регенерация (от лат. regeneratio - возрождение) - восстановление (возмещение) структурных элементов ткани взамен погибших. В биологическом смысле регенерация представляет собой приспособительный процесс, выработанный в ходе эволюции и присущий всему живому. В жизнедеятельности организма каждое функциональное отправление требует затрат материального субстрата и его восстановления. Следовательно, при регенерации происходит самовоспроизведение живой материи, причем это самовоспроизведение живого отражает принцип ауторегуляции и автоматизации жизненных отправлений (Давыдовский И.В., 1969).
Регенераторное восстановление структуры может происходить на разных уровнях - молекулярном, субклеточном, клеточном, тканевом и органном, однако всегда речь идет о возмещении структуры, которая способна выполнять специализированную функцию. Регенерация - это восстановление как структуры, так и функции. Значение регенераторного процесса - в материальном обеспечении гомеостаза.
Восстановление структуры и функции может осуществляться с помощью клеточных или внутриклеточных гиперпластических процессов. На этом основании различают клеточную и внутриклеточную формы регенерации (Саркисов Д.С., 1977). Для клеточной формы регенерации характерно размножение клеток митотическим и амитотическим путем, для внутриклеточной формы, которая может быть органоидной и внутриорганоидной, - увеличение числа (гиперплазия) и размеров (гипертрофия) ультраструктур (ядра, ядрышек, митохондрий, рибосом, пластинчатого комплекса и т.д.) и их компонентов (см. рис. 5, 11, 15). Внутриклеточная форма регенерации является универсальной, так как она свойственна всем органам и тканям. Однако структурно-функциональная специализация органов и тканей в фило- и онтогенезе «отобрала» для одних преимущественно клеточнуую форму, для других - преимущественно или исключительно внутриклеточную, для третьих - в равной мере обе формы регенерации (табл. 5). Преобладание той или иной формы регенерации в определенных органах и тканях определяется их функциональным назначением, структурно-функциональной специализацией. Необходимость сохранения целостности покровов тела объясняет, например, преобладание клеточной формы регенерации эпителия как кожи, так и слизистых оболочек. Специализированная функция пирамидной клетки головного
мозга, как и мышечной клетки сердца, исключает возможность деления этих клеток и позволяет понять необходимость отбора в фило- и онтогенезе внутриклеточной регенерации как единственной формы восстановления данного субстрата.
Таблица 5. Формы регенерации в органах и тканях млекопитающих (по Саркисову Д.С., 1988)
Эти данные опровергают существовавшие до недавнего времени представления об утрате некоторыми органами и тканями млекопитающих способности к регенерации, о «плохо» и «хорошо» регенерирующих тканях человека, о том, что существует «закон обратной зависимости» между степенью дифференцировки тканей и способностью их к регенерации. В настоящее время установлено, что в ходе эволюции способность к регенерации в некоторых тканях и органах не исчезла, а приняла формы (клеточную или внутриклеточную), соответствующие их структурному и функциональному своеобразию (Саркисов Д.С., 1977). Таким образом, все ткани и органы обладают способностью к регенерации, различны лишь ее формы в зависимости от структурно-функциональной специализации ткани или органа.
Морфогенез регенераторного процесса складывается из двух фаз - пролиферации и дифференцировки. Особенно хорошо эти фазы выражены при клеточной форме регенерации. В фазу пролиферации размножаются молодые, недифференцированные клетки. Эти клетки называют камбиальными (от лат. cambium - обмен, смена), стволовыми клетками и клетками-предшественниками.
Для каждой ткани характерны свои камбиальные клетки, которые отличаются степенью пролиферативной активности и специализации, однако одна стволовая клетка может быть родоначальником нескольких видов
клеток (например, стволовая клетка кроветворной системы, лимфоидной ткани, некоторые клеточные представители соединительной ткани).
В фазу дифференцировки молодые клетки созревают, происходит их структурно-функциональная специализация. Та же смена гиперплазии ультраструктур их дифференцировкой (созреванием) лежит в основе механизма внутриклеточной регенерации.
Регуляция регенераторного процесса. Среди регуляторных механизмов регенерации различают гуморальные, иммунологические, нервные, функциональные.
Гуморальные механизмы реализуются как в клетках поврежденных органов и тканей (внутритканевые и внутриклеточные регуляторы), так и за их пределами (гормоны, поэтины, медиаторы, факторы роста и др.). К гуморальным регуляторам относят кейлоны (от греч. chalaino - ослаблять) - вещества, способные подавлять деление клеток и синтез ДНК; они обладают тканевой специфичностью. Иммунологические механизмы регуляции связаны с «регенерационной информацией», переносимой лимфоцитами. В связи с этим следует заметить, что механизмы иммунологического гомеостаза определяют и структурный гомеостаз. Нервные механизмы регенераторных процессов связаны прежде всего с трофической функцией нервной системы, а функциональные механизмы - с функциональным «запросом» органа, ткани, который рассматривается как стимул к регенерации.
Развитие регенераторного процесса во многом зависит от ряда общих и местных условий, или факторов. К общим следует отнести возраст, конституцию, характер питания, состояние обмена и кроветворения, к местным - состояние иннервации, крово- и лимфообращения ткани, пролиферативную активность ее клеток, характер патологического процесса.
Классификация. Различают три вида регенерации: физиологическую, репаративную и патологическую.
Физиологическая регенерация совершается в течение всей жизни и характеризуется постоянным обновлением клеток, волокнистых структур, основного вещества соединительной ткани. Нет таких структур, которые не подвергались бы физиологической регенерации. Там, где доминирует клеточная форма регенерации, имеет место обновление клеток. Так происходит постоянная смена покровного эпителия кожи и слизистых оболочек, секреторного эпителия экзокринных желез, клеток, выстилающих серозные и синовиальные оболочки, клеточных элементов соединительной ткани, эритроцитов, лейкоцитов и тромбоцитов крови и т.д. В тканях и органах, где клеточная форма регенерации утрачена, например в сердце, головном мозге, происходит обновление внутриклеточных структур. Наряду с обновлением клеток и субклеточных структур постоянно совершается биохимическая регенерация, т.е. обновление молекулярного состава всех компонентов тела.
Репаративная или восстановительная регенерация наблюдается при различных патологических процессах, ведущих к повреждению клеток и тка-
ней. Механизмы репаративной и физиологической регенерации едины, репаративная регенерация - это усиленная физиологическая регенерация. Однако в связи с тем, что репаративная регенерация побуждается патологическими процессами, она имеет качественные морфологические отличия от физиологической. Репаративная регенерация может быть полной и неполной.
Полная регенерация, или реституция, характеризуется возмещением дефекта тканью, которая идентична погибшей. Она развивается преимущественно в тканях, где преобладает клеточная регенерация. Так, в соединительной ткани, костях, коже и слизистых оболочках даже относительно крупные дефекты органа могут путем деления клеток замещаться тканью, идентичной погибшей. При неполной регенерации, или субституции, дефект замещается соединительной тканью, рубцом. Субституция характерна для органов и тканей, в которых преобладает внутриклеточная форма регенерации, либо она сочетается с клеточной регенерацией. Поскольку при регенерации происходит восстановление структуры, способной к выполнению специализированной функции, смысл неполной регенерации не в замещении дефекта рубцом, а в компенсаторной гиперплазии элементов оставшейся специализированной ткани, масса которой увеличивается, т.е. происходит гипертрофия ткани.
При неполной регенерации, т.е. заживлении ткани рубцом, возникает гипертрофия как выражение регенераторного процесса, поэтому ее называют регенерационной, в ней - биологический смысл репаративной регенерации. Регенераторная гипертрофия может осуществляться двумя путями - с помощью гиперплазии клеток или гиперплазии и гипертрофии клеточных ультраструктур, т.е. гипертрофии клеток.
Восстановление исходной массы органа и его функции за счет преимущественно гиперплазии клеток происходит при регенерационной гипертрофии печени, почек, поджелудочной железы, надпочечников, легких, селезенки и др. Регенерационная гипертрофия за счет гиперплазии клеточных ультраструктур характерна для миокарда, головного мозга, т.е. тех органов, где преобладает внутриклеточная форма регенерации. В миокарде, например, по периферии рубца, заместившего инфаркт, размеры мышечных волокон значительно увеличиваются, т.е. они гипертрофируются в связи с гиперплазией их субклеточных элементов (рис. 81). Оба пути регенерационной гипертрофии не исключают друг друга, а, наоборот, нередко сочетаются. Так, при регенерационной гипертрофии печени происходит не только увеличение числа клеток в сохранившейся после повреждения части органа, но и гипертрофия их, обусловленная гиперплазией ультраструктур. Нельзя исключить того, что в мышце сердца регенерационная гипертрофия может протекать не только в виде гипертрофии волокон, но и путем увеличения числа составляющих их мышечных клеток.
Восстановительный период обычно не ограничивается только тем, что в поврежденном органе развертывается репаративная регенерация. Если
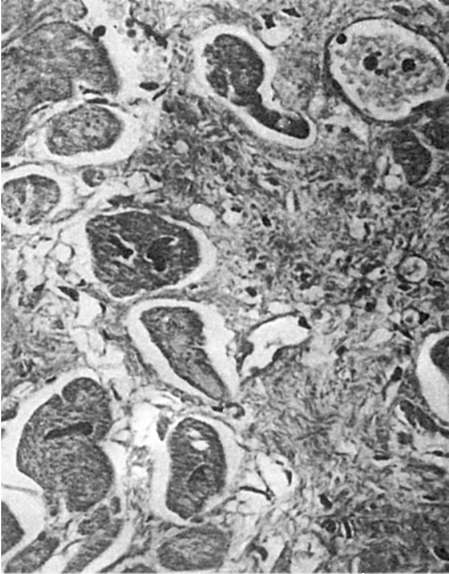 Рис. 81.
Регенерационная гипертрофия миокарда. По периферии рубца расположены гипертрофированные мышечные волокна
Рис. 81.
Регенерационная гипертрофия миокарда. По периферии рубца расположены гипертрофированные мышечные волокна
воздействие патогенного фактора прекращается до гибели клетки, происходит постепенное восстановление поврежденных органелл. Следовательно, проявления репаративной реакции должны быть расширены за счет включения восстановительных внутриклеточных процессов в дистрофически измененных органах. Общепринятое мнение о регенерации только как о завершающем этапе патологического процесса малооправданно. Репаративная регенерация не местная, а общая реакция организма, охватывающая различные органы, но реализующаяся в полной мере лишь в том или ином из них.
О патологической регенерации говорят в тех случаях, когда в результате тех или иных причин имеется извращение регенераторного процесса, нарушение смены фаз пролиферации
и дифференцировки. Патологическая регенерация проявляется в избыточном или недостаточном образовании регенерирующей ткани (гипер- или гипорегенерация), а также в превращении в ходе регенерации одного вида ткани в другой [метаплазия - см. Процессы приспособления (адаптации) и компенсации]. Примерами могут служить гиперпродукция соединительной ткани с образованием келоида, избыточная регенерация периферических нервов и избыточное образование костной мозоли при срастании перелома, вялое заживление ран и метаплазия эпителия в очаге хронического воспаления. Патологическая регенерация обычно развивается при нарушениях общих и местных условий регенерации (нарушение иннервации, белковое и витаминное голодание, хроническое воспаление и т.д.).
Регенерация отдельных тканей и органов
Репаративная регенерация крови отличается от физиологической прежде всего своей большей интенсивностью. При этом активный красный костный мозг появляется в длинных трубчатых костях на месте жирового костного мозга (миелоидное превращение жирового костного мозга). Жировые клетки вытесняются растущими островками кроветворной ткани, которая заполняет костномозговой канал и выглядит сочной, темнокрасной. Кроме того, кроветворение начинает происходить вне костного мозга - внекостномозговое, или экстрамедуллярное, кроветворение. Оча-
ги экстрамедуллярного (гетеротопического) кроветворения в результате выселения из костного мозга стволовых клеток появляются во многих органах и тканях - селезенке, печени, лимфатических узлах, слизистых оболочках, жировой клетчатке и т.д.
Регенерация крови может быть резко угнетена (например, при лучевой болезни, апластической анемии, алейкии, агранулоцитозе) или извращена (например, при злокачественной анемии, полицитемии, лейкозе). В кровь при этом поступают незрелые, функционально неполноценные и быстро разрушающиеся форменные элементы. В таких случаях говорят о патологической регенерации крови.
Репаративные возможности органов кроветворной и иммунокомпетентной системы неоднозначны. Костный мозг обладает очень высокими пластическими свойствами и может восстанавливаться даже при значительных повреждениях. Лимфатические узлы хорошо регенерируют только в тех случаях, когда сохраняются связи приносящих и выносящих лимфатических сосудов с окружающей их соединительной тканью. Регенерация ткани селезенки при повреждении бывает, как правило, неполной, погибшая ткань замещается рубцом.
Регенерация кровеносных и лимфатических сосудов протекает неоднозначно в зависимости от их калибра.
Микрососуды обладают большей способностью регенерировать, чем крупные сосуды. Новообразование микрососудов может происходить путем почкования или аутогенно. При регенерации сосудов путем почкования (рис. 82) в их стенке появляются боковые выпячивания за счет усиленно делящихся эндотелиальных клеток (ангиобласты). Образуются тяжи из эндотелия, в которых возникают просветы и в них поступает кровь или лимфа из «материнского» сосуда. Другие элементы: сосудистой стенки образуются за счет дифференцировки эндотелия и окружающих сосуд соединительнотканных клеток, В сосудистую стенку врастают нервные волокна из предсуществующих нервов. Аутогенное новообразование сосудов состоит в том, что в соединительной ткани появляются очаги недифференцированных клеток. В этих очагах возникают щели, в которые открываются предсуществующие капилляры и изливается кровь. Молодые клетки соединительной ткани, дифференцируясь, образуют эндотелиальную выстилку и другие элементы стенки сосуда.
 Рис. 82.
Регенерация сосудов путем почкования
Рис. 82.
Регенерация сосудов путем почкования
Крупные сосуды не обладают достаточными пластическими свойствами. Поэтому при повреждении их стенки восстанавливаются лишь структуры внутренней оболочки, ее эндотелиальная выстилка; элементы средней и наружной оболочек обычно замещаются соединительной тканью, что ведет нередко к сужению или облитерации просвета сосуда.
Регенерация соединительной ткани начинается с пролиферации молодых мезенхимальных элементов и новообразования микрососудов. Образуется молодая, богатая клетками и тонкостенными сосудами соединительная ткань, которая имеет характерный вид. Это - сочная темнокрасная ткань с зернистой, как бы усыпанной крупными гранулами поверхностью, что явилось основанием назвать ее грануляционной тканью. Гранулы представляют собой выступающие над поверхностью петли новообразованных тонкостенных сосудов, которые составляют основу грануляционной ткани. Между сосудами много недифференцированных лимфоцитоподобных клеток соединительной ткани, лейкоцитов, плазматических клеток и лаброцитов (рис. 83). В дальнейшем происходит созревание грануляционной ткани, в основе которой лежит дифференцировка клеточных элементов, волокнистых структур, а также сосудов. Число гематогенных элементов уменьшается, а фибробластов - увеличивается. В связи с синтезом фибробластами коллагена в межклеточных пространствах образуются аргирофильные (см. рис. 83), а затем и коллагеновые волокна. Синтез фибробластами гликозаминогликанов служит образованию
основного вещества соединительной ткани. По мере созревания фибробластов количество коллагеновых волокон увеличивается, они группируются в пучки; одновременно уменьшается количество сосудов, они дифференцируются в артерии и вены. Созревание грануляционной ткани завершается образованием грубоволокнистой рубцовой ткани.
Новообразование соединительной ткани происходит не только при ее повреждении, но и при неполной регенерации других тканей, а также при организации (инкапсуляции), заживлении ран, продуктивном воспалении.
Созревание грануляционной ткани может иметь те или иные отклонения. Воспаление, развивающееся в грануляционной ткани, приводит к задержке ее созревания,
 Рис. 83.
Грануляционная
ткань. Между тонкостенными сосудами много недифференцированных клеток
соединительной ткани и аргирофильных волокон. Импрегнация серебром
Рис. 83.
Грануляционная
ткань. Между тонкостенными сосудами много недифференцированных клеток
соединительной ткани и аргирофильных волокон. Импрегнация серебром
а чрезмерная синтетическая активность фибробластов - к избыточному образованию коллагеновых волокон с последующим резко выраженным их гиалинозом. В таких случаях возникает рубцовая ткань в виде опухолевидного образования синюшно-красного цвета, которая возвышается над поверхностью кожи в виде келоида. Келоидные рубцы образуются после различных травматических поражений кожи, особенно после ожогов.
Регенерация жировой ткани происходит за счет новообразования соединительнотканных клеток, которые превращаются в жировые (адипозоциты) путем накопления в цитоплазме липидов. Жировые клетки складываются в дольки, между которыми располагаются соединительнотканные прослойки с сосудами и нервами. Регенерация жировой ткани может происходить также из ядросодержащих остатков цитоплазмы жировых клеток.
Регенерация костной ткани при переломе костей в значительной мере зависит от степени разрушения кости, правильной репозиции костных отломков, местных условий (состояние кровообращения, воспаление и т.д.). При неосложненном костном переломе, когда костные отломки неподвижны, может происходить первичное костное сращение (рис. 84). Оно начинается с врастания в область дефекта и гематомы между отломками кости молодых мезенхимальных элементов и сосудов. Возникает так называемая предварительная соединительнотканная мозоль, в которой сразу же начинается образование кости. Оно связано с активацией и пролиферацией остеобластов в зоне повреждения, но прежде всего в периостате и эндостате. В остеогенной фиброретикулярной ткани появляются малообызвествленные костные балочки, число которых нарастает.
Образуется предварительная костная мозоль. В дальнейшем она созревает и превращается в зрелую пластинчатую кость - так образуется
 Рис. 84.
Первичное костное сращение. Интермедиарная костная мозоль (показана стрелкой), спаивающая отломки кости (по Г.И. Лаврищевой)
Рис. 84.
Первичное костное сращение. Интермедиарная костная мозоль (показана стрелкой), спаивающая отломки кости (по Г.И. Лаврищевой)
окончательная костная мозоль, которая по своему строению отличается от костной ткани лишь беспорядочным расположением костных перекладин. После того как кость начинает выполнять свою функцию и появляется статическая нагрузка, вновь образованная ткань с помощью остеокластов и остеобластов подвергается перестройке, появляется костный мозг, восстанавливаются васкуляризация и иннервация. При нарушении местных условий регенерации кости (расстройство кровообращения), подвижности отломков, обширных диафизарных переломах происходит вторичное костное сращение (рис. 85). Для этого вида костного сращения характерно образование между костными отломками сначала хрящевой ткани, на основе которой строится костная ткань. Поэтому при вторичном костном сращении говорят о предварительной костно-хрящевой мозоли, которая со временем превращается в зрелую кость. Вторичное костное сращение по сравнению с первичным встречается значительно чаще и занимает больше времени.
При неблагоприятных условиях регенерация костной ткани может быть нарушена. Так, при инфицировании раны регенерация кости задерживается. Костные осколки, которые при нормальном течении регенераторного процесса выполняют функцию каркаса для новообразованной костной ткани, в условиях нагноения раны поддерживают воспаление, что тормозит регенерацию. Иногда первичная костно-хрящевая мозоль не дифференцируется в костную. В этих случаях концы сломанной кости остаются подвижными, образуется ложный сустав. Избыточная продукция костной ткани в ходе регенерации приводит к появлению костных выростов - экзостозов.
Регенерация хрящевой ткани в отличие от костной происходит обычно неполно. Лишь небольшие дефекты ее могут замещаться новообразованной тканью за счет камбиальных элементов надхрящницы - хондробластов. Эти клетки создают основное вещество хряща, затем превращаются в зрелые хрящевые клетки. Крупные дефекты хряща замещаются рубцовой тканью.
Регенерация мышечной ткани, ее возможности и формы различны в зависимости от вида этой ткани. Гладкие мьшщы, клетки которых обладают способностью к митозу и амитозу, при незначительных дефектах могут регенерировать достаточно полно. Значительные участки повреждения гладких мышц замещаются рубцом, при этом сохранившиеся мышечные волокна подвергаются гипертрофии. Новообразование гладких мышечных волокон может происходить путем превращения (метаплазии) элементов соединительной ткани. Так образуются пучки гладких мышечных волокон в плевральных спайках, в подвергающихся организации тромбах, в сосудах при их дифференцировке.
Поперечнополосатые мышцы регенерируют лишь при сохранении сарколеммы. Внутри трубок из сарколеммы осуществляется регенерация ее органелл, в результате чего появляются клетки, называемые миобластами. Они вытягиваются, число ядер в них увеличивается, в саркоплазме
 Рис. 85.
Вторичное костное сращение (по Г.И. Лаврищевой):
Рис. 85.
Вторичное костное сращение (по Г.И. Лаврищевой):
а - костно-хрящевая периостальная мозоль; участок костной ткани среди хрящевой (микроскопическая картина); б - периостальная костно-хрящевая мозоль (гистотопограмма через 2 мес после операции): 1 - костная часть; 2 - хрящевая часть; 3 - отломки кости; в - периостальная мозоль, спаивающая смещенные отломки кости
дифференцируются миофибриллы, и трубки сарколеммы превращаются в поперечнополосатые мышечные волокна. Регенерация скелетных мышц может быть связана и с клетками-сателлитами, которые располагаются под сарколеммой, т.е. внутри мышечного волокна, и являются камбиальными. В случае травмы клетки-сателлиты начинают усиленно делиться, затем подвергаются дифференцировке и обеспечивают восстановление мышечных волокон. Если при повреждении мышцы целость волокон нарушается, то на концах их разрывов возникают колбообразные выбухания, которые содержат большое число ядер и называются мышечными почками. При этом восстановления непрерывности волокон не происходит. Место разрыва заполняется грануляционной тканью, превращающейся в рубец (мышечная мозоль). Регенерация мышцы сердца при ее повреждении, как и при повреждении поперечнополосатой мускулатуры, заканчивается рубцеванием дефекта. Однако в сохранившихся мышечных волокнах происходит интенсивная гиперплазия ультраструктур, что ведет к гипертрофии волокон и восстановлению функции органа (см. рис. 81).
Регенерация эпителия осуществляется в большинстве случаев достаточно полно, так как он обладает высокой регенераторной способностью. Особенно хорошо регенерирует покровный эпителий. Восстановление многослойного плоского ороговевающего эпителия возможно даже при довольно крупных дефектах кожи. При регенерации эпидермиса в краях дефекта происходит усиленное размножение клеток зародышевого (камбиального), росткового (мальпигиева) слоя. Образующиеся эпителиальные клетки сначала покрывают дефект одним слоем. В дальнейшем пласт эпителия становится многослойным, клетки его дифференцируются, и он приобретает все признаки эпидермиса, включающего в себя ростковый, зернистый блестящий (на подошвах и ладонной поверхности кистей) и роговой слои. При нарушении регенерации эпителия кожи образуются незаживающие язвы, нередко с разрастанием в их краях атипичного эпителия, что может послужить основой для развития рака кожи.
Покровный эпителий слизистых оболочек (многослойный плоский неороговевающий, переходный, однослойный призматический и многоядерный мерцательный) регенерирует таким же образом, как и многослойный плоский ороговевающий. Дефект слизистой оболочки восстанавливается за счет пролиферации клеток, выстилающих крипты и выводные протоки желез. Недифференцированные уплощенные клетки эпителия сначала покрывают дефект тонким слоем (рис. 86), затем клетки принимают форму, свойственную клеточным структурам соответствующей эпителиальной выстилки. Параллельно частично или полностью восстанавливаются и железы слизистой оболочки (например, трубчатые железы кишки, железы эндометрия).
Регенерация мезотелия брюшины, плевры и околосердечной сумки осуществляется путем деления сохранившихся клеток. На поверхности дефекта появляются сравнительно крупные кубические клетки, которые затем уплощаются. При небольших дефектах мезотелиальная выстилка восстанавливается быстро и полно.
Важное значение для восстановления покровного эпителия и мезотелия имеет состояние подлежащей соединительной ткани, так как эпителизация любого дефекта возможна лишь после заполнения его грануляционной тканью.
Регенерация специализированного эпителия органов (печени, поджелудочной железы, почек, желез внутренней секреции, легочных альвеол) осуществляется по типу регенерационной гипертрофии: в участках повреждения ткань замещается рубцом, а по периферии его происходят гиперплазия и гипертрофия клеток паренхимы. В печени участок некроза всегда подвергается рубцеванию, однако в остальной части органа происходит интенсивное новообразование клеток, а также гиперплазия внутриклеточных стуктур, что сопровождается их гипертрофией. В результате этого исходная масса и функция органа быстро восстанавливаются. Регенераторные возможности печени почти безграничны. В поджелудочной железе регенераторные процессы хорошо выражены как в экзокринных отделах, так и в панкреатических островках, причем эпителий экзокринных желез становится источником восстановления островков. В почках при некрозе эпителия канальцев происходит размножение сохранившихся нефроцитов и восстановление канальцев, однако лишь при сохранении тубулярной базальной мембраны. При ее разрушении (тубулорексис) эпителий не восстанавливается и каналец замещается соединительной тканью. Не восстанавливается погибший канальцевый эпителий и в том случае, когда одновременно с канальцем погибает сосудистый клубочек. При этом на месте погибшего нефрона разрастается рубцовая соединительная ткань, а окружающие нефроны подвергаются регенерационной гипертрофии. В железах внутренней секреции восстановительные процессы также представлены неполной регенерацией. В легком после удаления отдельных долей в оставшейся части происходит гипертрофия и гиперплазия тканевых элементов. Регенерация специализированного эпителия органов может протекать атипично, что ведет к разрастанию соединительной ткани, структурной перестройке и деформации органов; в таких случаях говорят о циррозе (цирроз печени, нефроцирроз, пневмоцирроз).
Регенерация разных отделов нервной системы происходит неоднозначно. В головном и спинном мозге новообразования ганглиозных клеток не про-
 Рис. 86.
Регенерация эпителия в дне хронической язвы желудка
Рис. 86.
Регенерация эпителия в дне хронической язвы желудка
исходит и при разрушении их восстановление функции возможно лишь за счет внутриклеточной регенерации сохранившихся клеток. Невроглии, особенно микроглии, свойственна клеточная форма регенерации, поэтому дефекты ткани головного и спинного мозга обычно заполняются пролиферирующими клетками невроглии - возникают так называемые глиальные (глиозные) рубцы. При повреждении вегетативных узлов наряду с гиперплазией ультраструктур клеток происходит и их новообразование. При нарушении целости периферического нерва регенерация происходит за счет центрального отрезка, сохранившего связь с клеткой, в то время как периферический отрезок погибает. Размножающиеся клетки шванновской оболочки погибшего периферического отрезка нерва располагаются вдоль него и образуют футляр - так называемый бюнгнеровский тяж, в который врастают регенерирующие осевые цилиндры из проксимального отрезка. Регенерация нервных волокон завершается их миелинизацией и восстановлением нервных окончаний. Регенерационная гиперплазия рецепторов, перицеллюлярных синаптических приборов и эффекторов иногда сопровождается гипертрофией их концевых аппаратов. Если регенерация нерва в силу тех или иных причин нарушается (значительное расхождение частей нерва, развитие воспалительного процесса), то в месте его перерыва образуется рубец, в котором беспорядочно располагаются регенерировавшие осевые цилиндры проксимального отрезка нерва. Аналогичные разрастания возникают на концах перерезанных нервов в культе конечности после ее ампутации. Такие разрастания, образованные нервными волокнами и фиброзной тканью, называются ампутационными невромами.
Заживление ран
Заживление ран протекает по законам репаративной регенерации. Темпы заживления ран, его исходы зависят от степени и глубины раневого повреждения, структурных особенностей органа, общего состояния организма, применяемых методов лечения. По И.В. Давыдовскому, выделяют следующие виды заживления ран: 1) непосредственное закрытие дефекта эпителиального покрова; 2) заживление под струпом; 3) заживление раны первичным натяжением; 4) заживление раны вторичным натяжением, или заживление раны через нагноение.
Непосредственное закрытие дефекта эпителиального покрова - это простейшее заживление, заключающееся в наползании эпителия нд поверхностный дефект и закрытии его эпителиальным слоем. Наблюдаемое на роговице, слизистых оболочках заживление под струпом касается мелких дефектов, на поверхности которых быстро возникает подсыхающая корочка (струп) из свернувшейся крови и лимфы; эпидермис восстанавливается под корочкой, которая отпадает через 3-5 сут после ранения.
Заживление первичным натяжением (per rimamm intentionem) наблюдается в ранах с повреждением не только кожи, но и подлежащей ткани,
причем края раны ровные. Рана заполняется свертками излившейся крови, что предохраняет края раны от дегидратации и инфекции. Под влиянием протеолитических ферментов неитрофилов происходит частичный лизис свертка крови, тканевого детрита. Нейтрофилы погибают, на смену им приходят макрофаги, которые фагоцитируют эритроциты, остатки поврежденной ткани; в краях раны обнаруживается гемосидерин. Часть содержимого раны удаляется в первый день ранения вместе с экссудатом самостоятельно или при обработке раны - первичное очищение. На 2-3-и сутки в краях раны появляются растущие навстречу друг другу фибробласты и новообразованные капилляры, появляется грануляционная ткань, пласт которой при первичном натяжении не достигает больших размеров. К 10-15-м суткам она полностью созревает, раневой дефект эпителизируется и рана заживает нежным рубчиком. В хирургической ране заживление первичным натяжением ускоряется в связи с тем, что ее края стягиваются нитями шелка или кетгута, вокруг которых скапливаются рассасывающие их гигантские клетки инородных тел, не мешающие заживлению.
Заживление вторичным натяжением (per secundam intentionem), или заживление через нагноение (или заживление посредством гранулирования - per granulationem), наблюдается обычно при обширных ранениях, сопровождающихся размозжением и омертвением тканей, проникновении в рану инородных тел, микробов. На месте раны возникают кровоизлияния, травматический отек краев раны, быстро появляются признаки демаркационного гнойного воспаления на границе с омертвевшей тканью, расплавление некротических масс. В течение первых 5-6 сут происходит отторжение некротических масс - вторичное очищение раны, и в краях раны начинает развиваться грануляционная ткань. Грануляционная ткань, выполняющая рану, состоит из 6 переходящих друг в друга слоев (Аничков Н.Н., 1951): поверхностный лейкоцитарно-некротический слой; поверхностный слой сосудистых петель, слой вертикальных сосудов, созревающий слой, слой горизонально расположенных фибробластов, фиброзный слой. Созревание грануляционной ткани при заживлении раны вторичным натяжением сопровождается регенерацией эпителия. Однако при этом виде заживления раны на месте ее всегда образуется рубец.